双刊连发!温医大眼视光池在龙团队解析姜黄类囊泡干预眼病新路径
缺血性视网膜病变以及干眼症等发病机制复杂,临床上以对症治疗为主,严重困扰患者生活质量,且近年来呈逐年增长的趋势。眼部缺血缺氧和慢性炎症等诱发局部微环境稳态平衡破坏,导致视功能损害甚至不可逆失明。目前治疗仍不能满足临床需求,鉴于疾病的复杂性及单靶点治疗的局限性,亟待探索多靶点调控潜力的新型干预策略。中草药的多成分、多靶点、多途径作用特征是复杂性疾病治疗的优势所在。细胞外囊泡(EVs)是纯天然的纳米级囊泡,可携带生物活性分子,是细胞间信息传递的重要介质。植物来源类囊泡(EVLPs)在形态、组成和功能上与哺乳动物EVs相似,能在物种之间交换生物信息,因其来源广、产率高、活性明显等优点受到广泛关注。中草药囊泡(CHM-EVLPs)来源于天然植物,具有多组分、多功能的特点,容易被生物体吸收,可以作为生物治疗剂和药物递送载体,有助于解决许多活性成分生物利用度差的问题,且具有更好的生物安全性。
近日,视觉健康全国重点实验室、温州医科大学附属眼视光医院池在龙团队在Journal of Nanobiotechnology杂志上(1区TOP期刊)在线发表了题为“Curcuma longa-Derived Extracellular Vesicle-Like Particles Ameliorate Retinal Neovascularization through HIF-1α and NRF2 signaling”的研究论文。该研究揭示了姜黄来源类囊泡(CL-EVLPs)在缺血性视网膜病变模型中的抗炎抗氧化及抑制新生血管的作用,并阐明了改善视网膜病理性新生血管的潜在机制。温州医科大学池在龙研究员为通讯作者,2022级硕士研究生陈颖和彭德伟副研究员为共同第一作者。
【文章要点】
从 Curcuma longa 粗提液中提取 CL-EVLPs(图1A),利用透射电子显微镜观察超微结构(图1B),纳米颗粒跟踪分析测定其粒径分布和颗粒浓度(图1C),蛋白印迹法检测标志蛋白(图1D)。CL-EVLPs内容物代谢组学分析发现检出的代谢产物中有Curcumin(姜黄素)、Auraptene(橙皮油素)、Triptophenolide‌(山海棠素、雷酚内酯)等一千多种小分子化合物(图1E)。
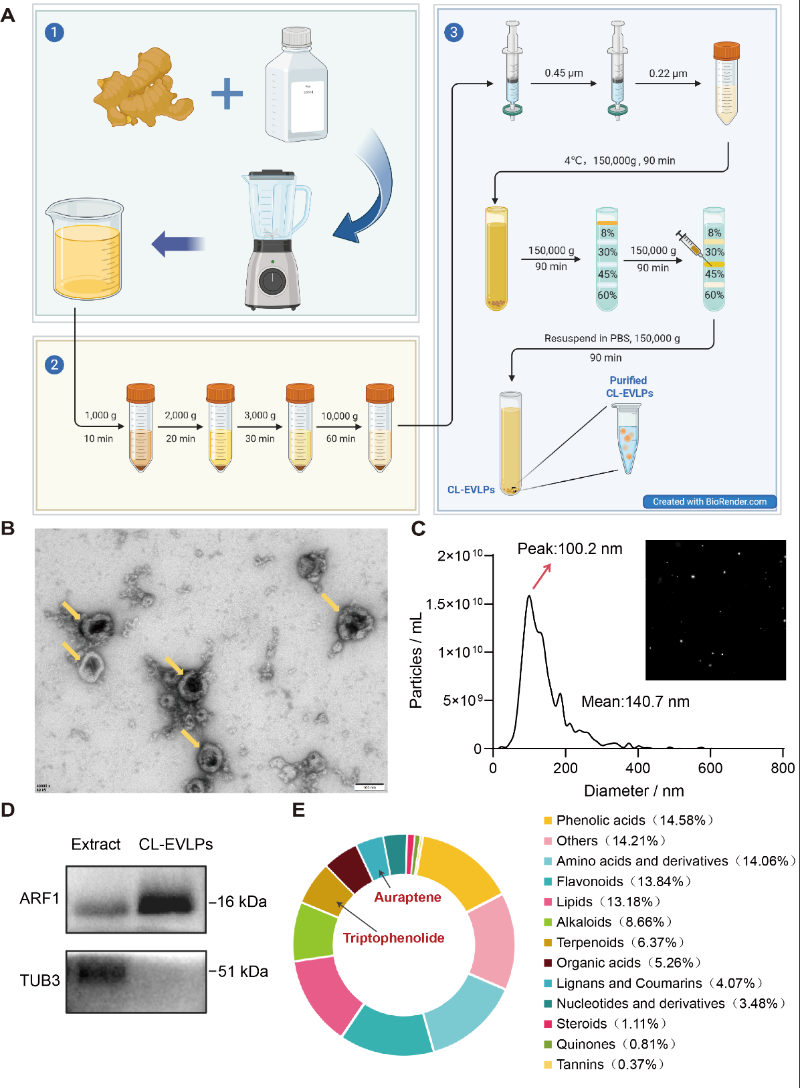
图1. CL-EVLPs提取及表征
小鼠 OIR 模型是经典且常用的缺血性视网膜病变模型,表现为明显的无血管区和病理性新生血管形成。利用红色荧光染料DiD标记CL-EVLPs 后行小鼠玻璃体腔内注射,发现被视网膜组织摄取良好(图2A-B)。继而小鼠 OIR 模型干预实验表明,CL-EVLPs 可显著缩小无血管区面积并抑制病理性新生血管生成(图2C-F)。
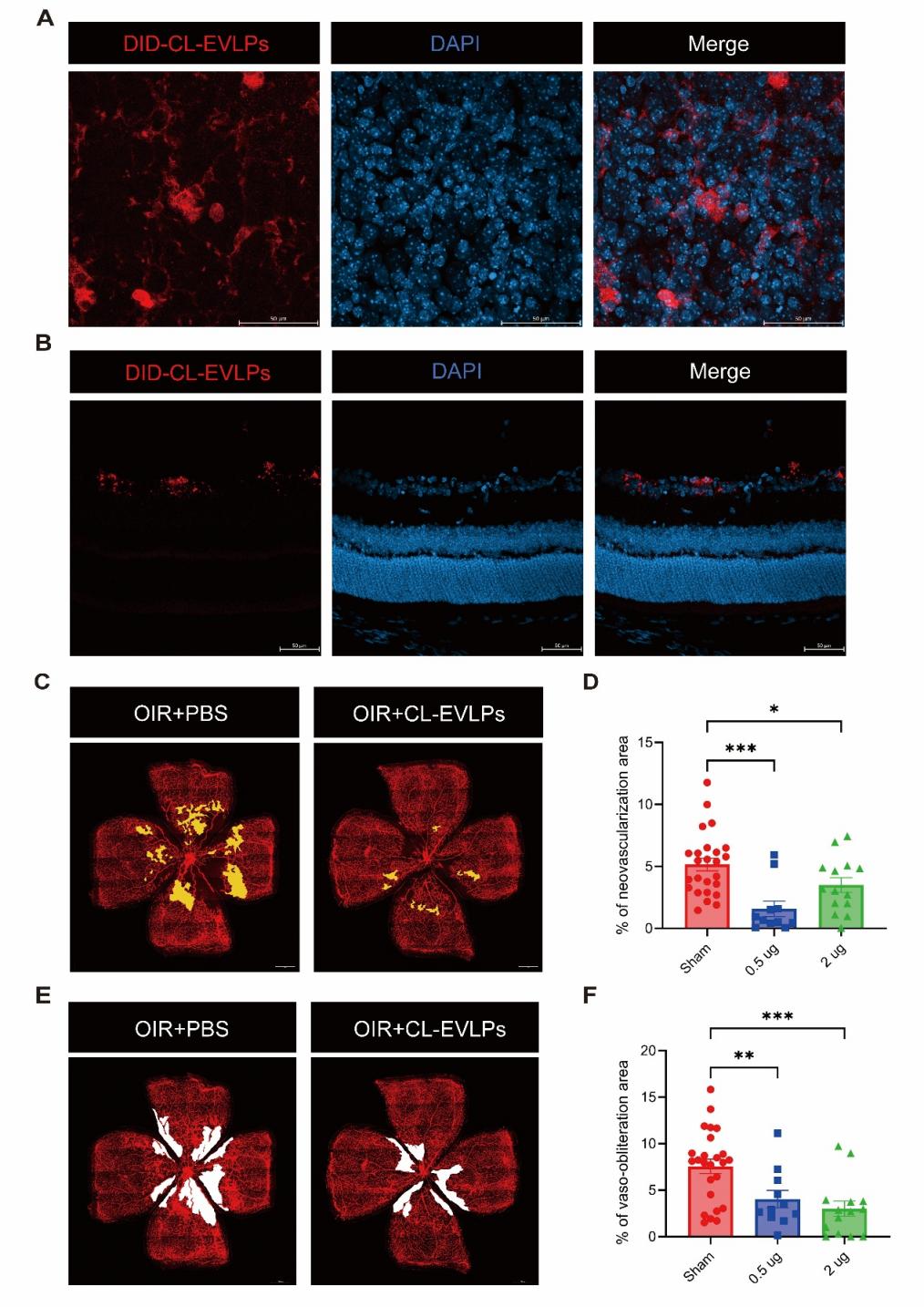
图2. CL-EVLPs抑制OIR小鼠视网膜病理性新生血管生成
为了明确CL-EVLPs的干预作用机制,该研究开展了视网膜组织转录组学测序分析,结果显示差异表达基因显著富集于细胞缺氧感应的HIF信号等通路(图3A-C)。进一步定量实验表明CL-EVLPs上调Egl-9家族缺氧诱导因子1(Egln1)的表达(图3D),该基因可通过von Hippel-Lindau泛素化复合物靶向HIF亚基进行蛋白酶体破坏。同时,验证了CL-EVLPs显著抑制HIF-1α,p-NF-κB p65和VEGFA蛋白的表达(图3E-H)。CL-EVLPs可能通过缺氧应答网络调控炎症信号激活并抑制新生血管生成。
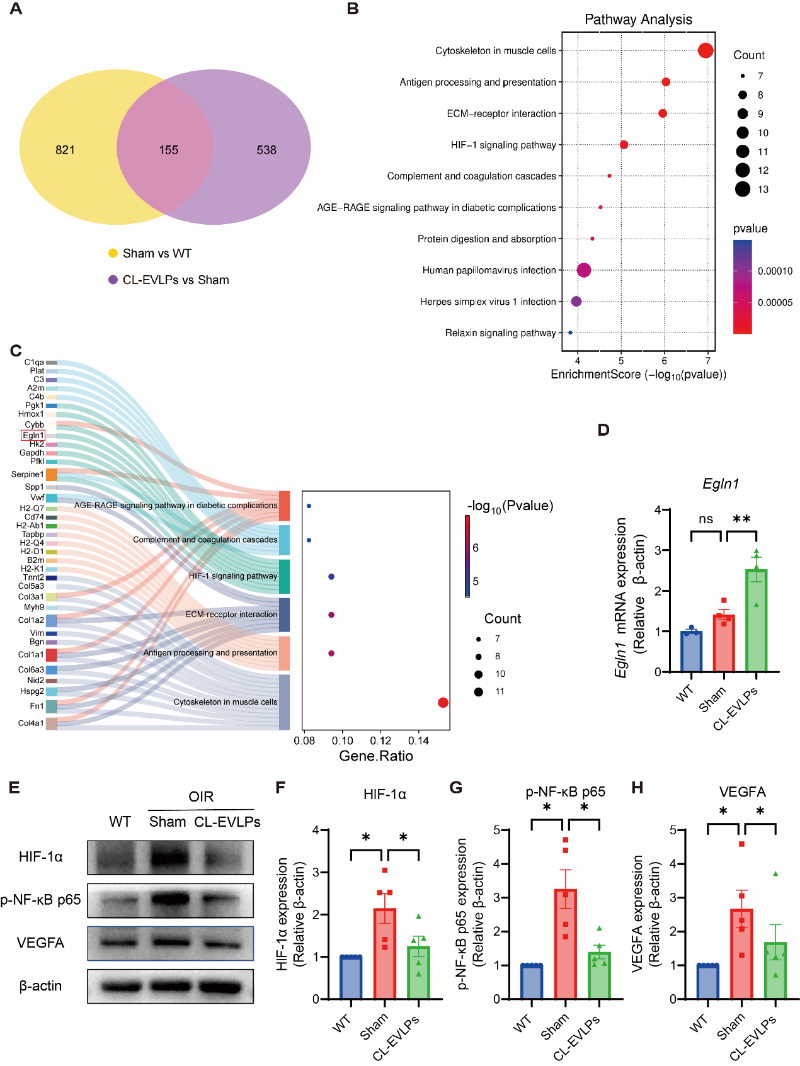
图3. CL-EVLPs抑制HIF通路
鉴于CL-EVLPs在抗氧化应激方面显示出的潜能,进一步实验验证了抗氧化相关信号通路。在 OIR 小鼠视网膜中,CL-EVLPs明显促进 NRF2 进入细胞核,并上调其下游抗氧化因子Ho-1表达(图4A-D)。体外实验亦表明CL-EVLPs促进小胶质细胞中NRF2的核转移,同时抑制氧化因子 Nos2 的表达,并上调抗氧化因子Ho-1和Cat的表达(图4E-J)。体内外实验均表明了CL-EVLPs能够增强视网膜组织对氧化应激损伤的抵御能力。
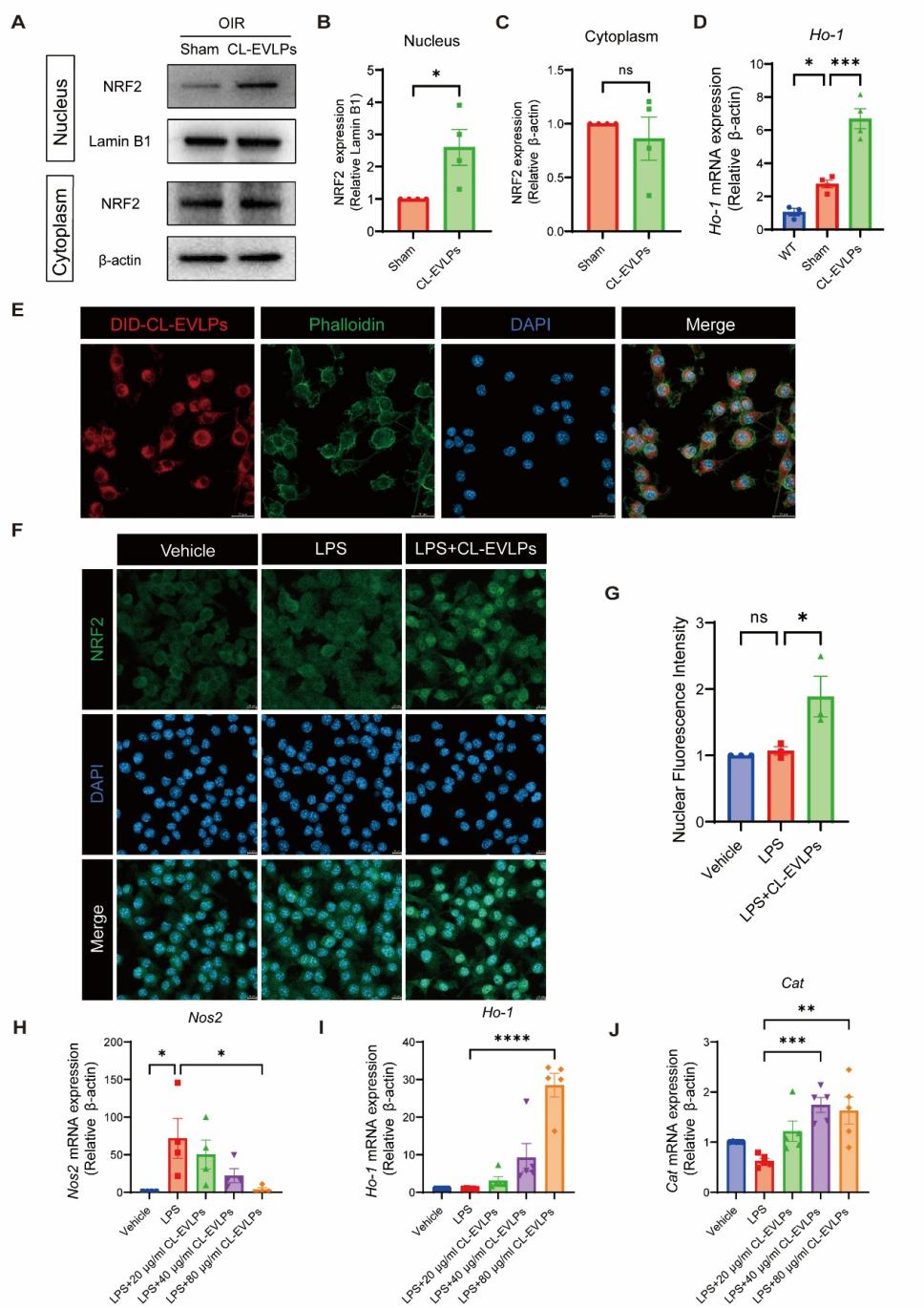
图4. CL-EVLPs激活NRF2/HO-1抗氧化通路
为了探究CL-EVLPs内容物中的哪个成分发挥作用,研究通过CL-EVLPs中高丰度化合物与OIR模型视网膜组织中差异代谢产物的交集,同时利用疾病靶基因数据库与小分子化合物预测调控靶基因数据库进行交集,发现相关生物学功能与信号通路富集于MAPK活性及PI3K-AKT通路等,印证了上述调控机制的发现(图5A-E)。图5F展示了两个生物活性分子Auraptene和Triptophenolide与靶基因的计算机模拟分子对接模型,CDK2、KIT和PIK3CA均富集于‌PI3K-AKT信号通路‌。进一步,体外实验亦证明了Auraptene和Triptophenolide的潜在作用(详见论文补充数据)。
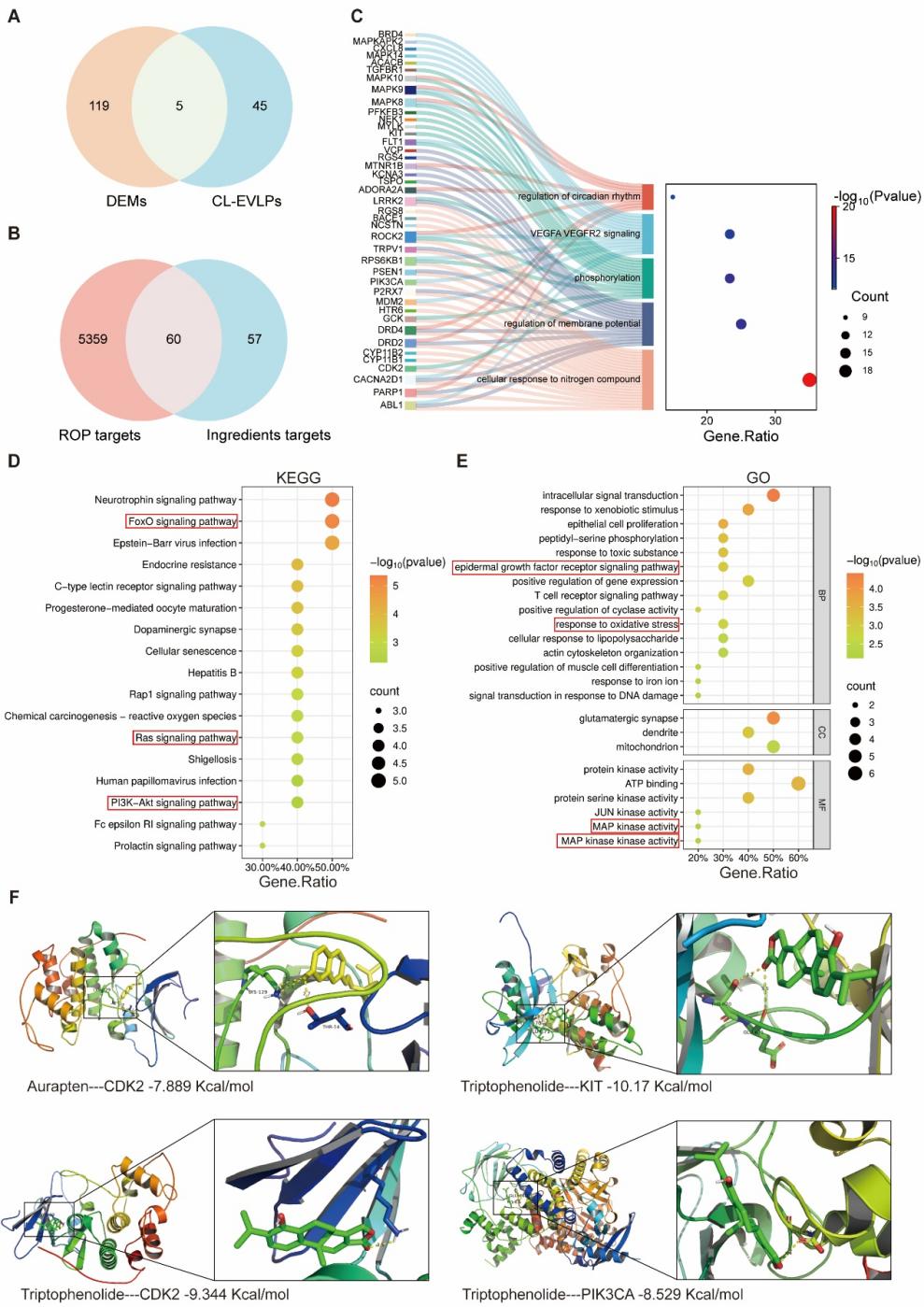
图5. CL-EVLPs内容物干预OIR模型的潜在机制分析
综上,该研究阐明了CL-EVLPs改善缺血性视网膜病变中的作用及潜在机制(图6),为植物或中草药来源类囊泡在眼病中的应用提供了新型治疗策略。未来仍需利用更多的动物模型等进一步探究其功能作用及长期安全性等,并探索与抗VEGF药物等联合应用的可能性。
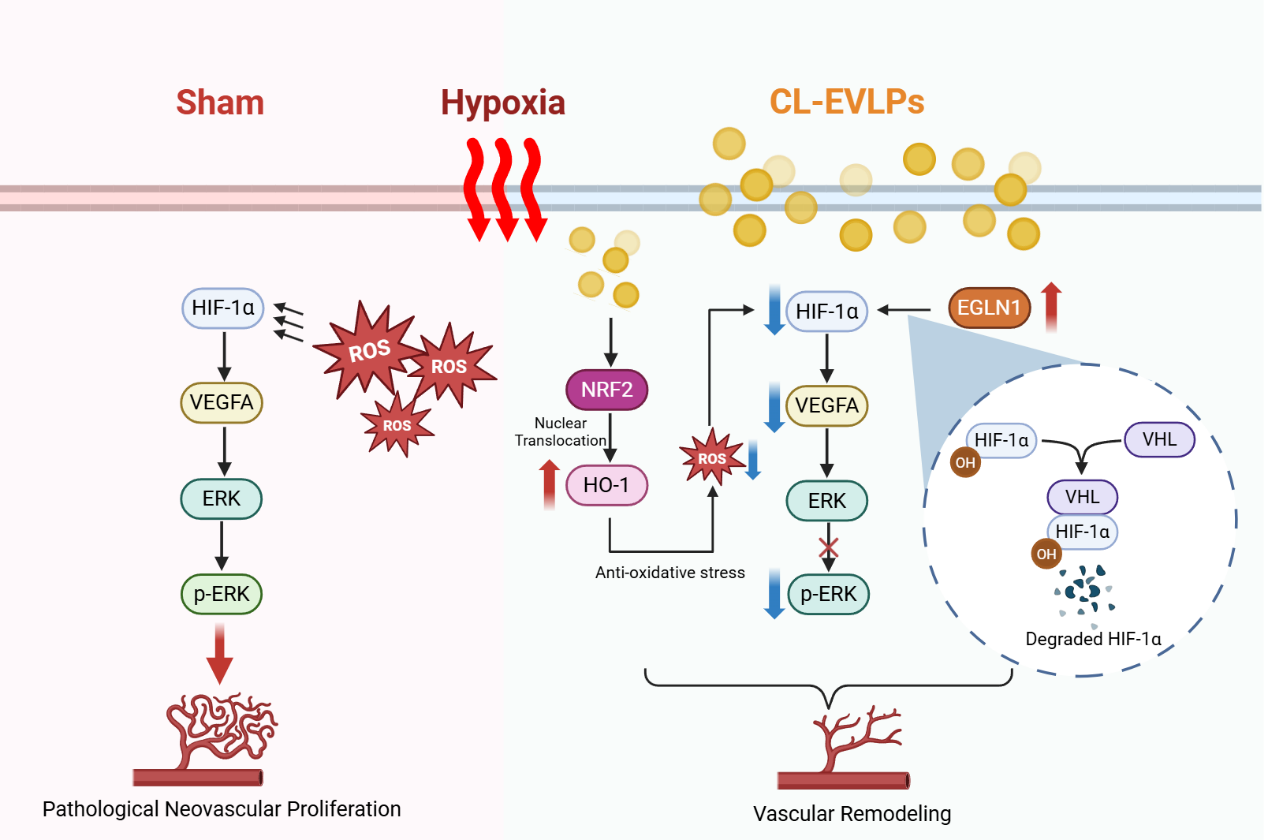
图6. CL-EVLPs干预缺血性视网膜病变的潜在机制示意图
【延伸阅读】
除本次针对缺血性视网膜病变的突破性研究外,池在龙研究员团队围绕姜黄来源类囊泡在眼病领域的干预价值,已开展系统性布局并取得系列成果。此前,团队率先在眼科TOP期刊Investigative Ophthalmology&Visual Science上发表题为“CL-EVLPs Promote Corneal Repair in a BAC-Induced Corneal Injury Model via Ocular Microenvironment Reconstruction”的前期研究成果,揭示了CL-EVLPs在苯扎氯铵诱导角膜损伤模型中的抗炎抗氧化、促神经修复及抑制新生血管的多重作用,并初探了改善角膜损伤修复的潜在机制。池在龙研究员为通讯作者,2022级博士研究生付梦君和彭德伟副研究员为共同第一作者。

【讨论与展望】
缺血性视网膜病变以及干眼综合征的病理机制复杂,因此单一靶点干预往往难以满足临床需求,严重危害患者身心健康。中医药是我国的瑰宝国粹之一,我们关注中草药的多靶点治疗及生物安全性等优势特征。中草药囊泡蕴含了中草药中绝大部分的活性成分,生物相容性好、且可大量提取等,具有很好的应用前景。CL-EVLPs展现出显著的抗炎抗氧化和微环境稳态维持等多靶点多通路调控作用,表明天然植物纳米囊泡在复杂眼病干预中的潜在优势。作为中医药学与现代科技结合的创新产物,中草药囊泡或可为创新药物的发现和应用开辟新的途径。
参考文献:
1. Chen Y, Peng DW, Jiang SR et al. Curcuma longa-derived extracellular vesicle-like particles ameliorate retinal neovascularization through HIF-1α and NRF2 signaling. J Nanobiotechnol. 2026 Mar 18.
2. Fu M, Peng D, Xu Y, Zhang Y, Chen Y, Shao Q, Chi ZL. CL-EVLPs Promote Corneal Repair in a BAC-Induced Corneal Injury Model via Ocular Microenvironment Reconstruction. Invest Ophthalmol Vis Sci. 2026 Mar 2; 67(3): 4. doi: 10.1167/iovs.67.3.4.
上一篇文章: @党支部 请查收2026年一季度党员教育学习资料包!
下一篇文章: 载誉而归!温医大眼视光学员在眼科学教育大会斩获多项荣誉